水合电子是什么东西?水合电子如何产生的?
这一现象弓I起了威尔的兴趣。
经过一番研究,他找出了其中的原因: 液态氨给出质子的能力比水弱,而钠又是较活泼的金属,它会在液态氨中 慢慢溶解,生成深蓝色溶液。
这种溶液的导电能力很强,和金属相近,这 是因为金属与液态氨作用形成了氨合电子和金属正离子的缘故。
他们 推断,既然有氨合电子的存在,自然就能找到神秘的水合电子。
经过近 一个世纪的努力,化学家斯蒂终于发现了水合电子的行踪。
在无机化学 中是指物质溶解在水里时,与水发生 的化学作用。
一般指溶质分子(或离 子)和水分子发生作用,形成水合分 子(或水合离子)的过程。
当时,斯蒂将甲基蓝溶液放在光照的条件下,发现溶液 的蓝色逐渐消失了。
奇怪的是,当他往溶液中通入二氧化碳气体后,蓝色又奇迹般地出现,斯蒂大惑不解,又重复了这一实验过程。
经过仔细分析,他最终推断:甲基蓝褪色是由于它和水合电子结合的缘故,通入二氧化碳后会复 原,是由于二氧化碳夺走了水合电子的缘故。
不久,斯蒂的推论又在实 验中得到了进一步的证实。
其化学性质十分活跃,可以说是目前已知还原剂中的最强者,它几乎能 与任何元素及化合物发生化学反应,还能与某些物质合成极难合成的物 质。
例如,通常情况下,三价的错离子很难转变成二价的铸离子,而假 如有水合电子的加入,这一还原反应就变得轻而易举了。
但是经过了几十年的研究,科学家们仍然不清楚水合电子的化学结构和应用前景。
看来要解开这个谜,仍需进一步探索。
水合电子还原降解全氟烷基化合物的结构
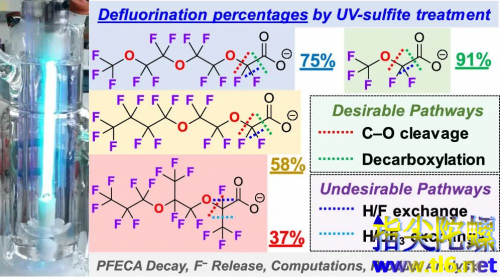
自上世纪40年代起,全氟烷基化合物(PFAS)凭借优异的疏水、疏油、热稳定等诸多独特性质,已被广泛应用在各类工业生产过程和日常生活用品中。
同时,高度稳定的碳氟键(C−F)导致PFAS难以被自然过程或现有工程处理技术降解,成为持久性环境污染物。
除了纯碳链结构的全氟羧酸(例如著名的全氟辛酸PFOA),碳链中插入醚键的全氟烷基醚羧酸(PFECA)作为PFOA的替代品已被大量生产和使用(例如最近被新闻广泛报道的GenX,图1)。
PFECA分子的设计合成比较灵活,被醚氧原子分隔的氟碳链可以有各种长度,既可以是直链,也可以有支链。
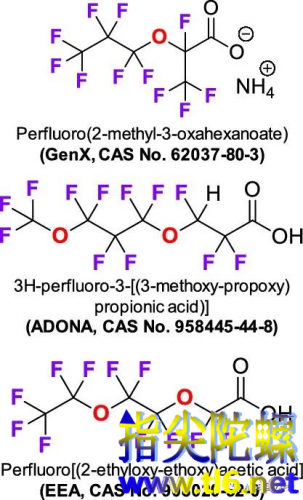
图1.三种已被报道的全氟/多氟烷基醚羧酸
在紫外光的激发下,亚硫酸根离子释放出高度还原性的水合电子(eaq−),可在室温下对PFAS进行深度还原降解(见摘要图)。
尽管我们稍早前的工作(10.1021/acs.est.8b06648)对eaq−用于纯碳链羧酸的还原降解进行了系统研究,但PFECA结构中醚氧原子的引入导致了全氟烷基片段的长度和C−F键能的显著改变,这种变化可能产生新的反应机理并导致不同的降解速率和脱氟程度。
为了给这类新型氟化物的降解处理提供理论指导,这项工作系统研究了4类共10种全氟烷基醚羧酸结构(见表1)的还原降解。
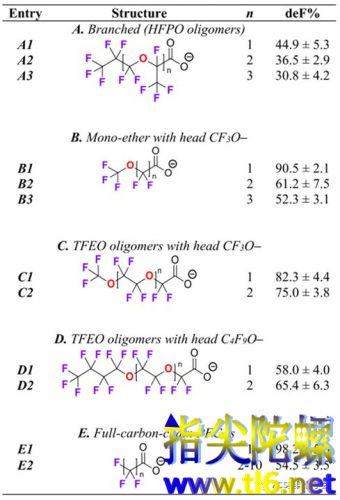
表1.四类全氟烷基醚羧酸(A−D)和全碳链羧酸(E)的结构及48h的脱氟率(deF%)
在相同的光化学反应条件下(25µMPFECA,10mMNa2SO3,5mMNaHCO3,pH9.5,18W254nm低压汞灯,20℃),这些PFECA化合物的降解和脱氟呈现出显著不同(图2)。
相比之下,不同链长的纯碳链羧酸(除了三氟乙酸)的降解表现非常相似。
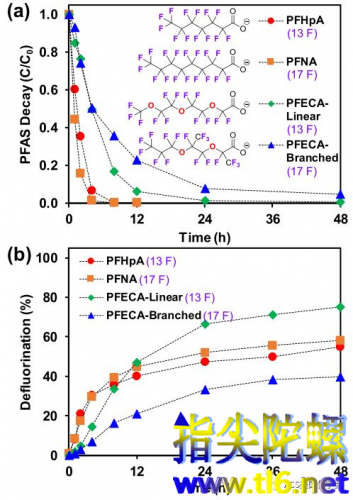
图2.两种PFECA和具有相同氟原子数的纯碳链羧酸的降解(a)和脱氟(b)之比较
对C−F键解离能的计算表明,较弱的C−F键存在于较长的氟碳链中段,以及紧邻羧基的α位碳上(图3)。
与纯碳链羧酸相比,直线型PFECA(表1的B、C、D类结构)醚氧原子的插入将长碳链分割为多个片段,这显著提高了几乎所有C−F的键能。
然而,这些直线型PFECA的脱氟率(52–90%)却与纯碳链羧酸的脱氟率(55%左右)类似甚至更高。
相反,支链型PFECA(表1的A类结构)三级碳上的C−F键能很低,但脱氟率(31–45%)却显著低于纯碳链羧酸。
这些结果与“弱C−F键越多,越有利于脱氟”的直观预测相违背。
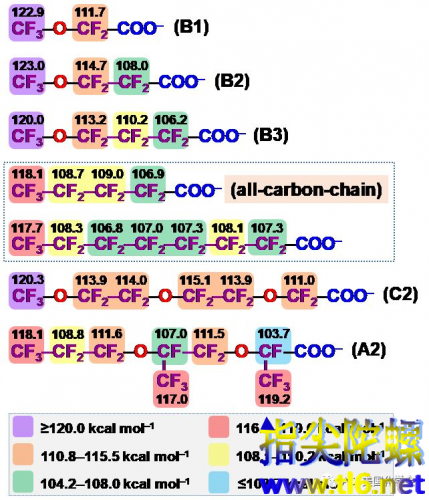
图3.PFECA中C−F键能与纯碳链羧酸中C−F键能的比较
另一个很有意思的发现是C−O键的解离能。
如图4所示,离羧基最近的醚官能团中有一个C−O键显著弱于其他所有的C−O键,即使这个醚官能团距离羧基较远(例如结构B3)也是如此。
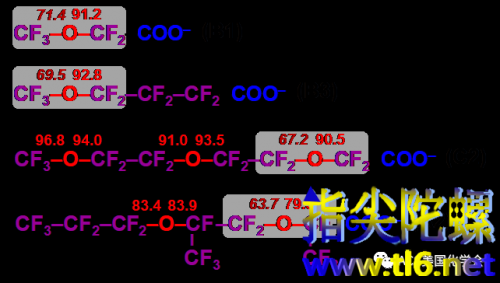
图4.PFECA分子中的C−O键能
当对这些PFECA阴离子外加一个电子(模拟与eaq−结合)后进行结构优化,一些PFECA结构的α位碳上的C−F键发生了自动解离,另一些结构中离羧基最近的C−O键发生了自动解离(图5)。
同时,我们用高分辨质谱对实际反应的样品进行了产物分析,发现了一系列分子骨架不变但出现H/F原子交换的产物,以及C−O键断裂后的产物。
这进一步印证了由模拟计算得出的两种脱氟途径。
C−O键断裂后,首先生成不稳定的全氟醇RF−CF2−OH,全氟醇自发分解,消除一个HF变成酰氟RF−C(O)−F,后者继续水解变为羧酸RF−C(O)O−,整个过程导致与羟基相连的碳原子上的C−F键全部断裂生成氟离子。
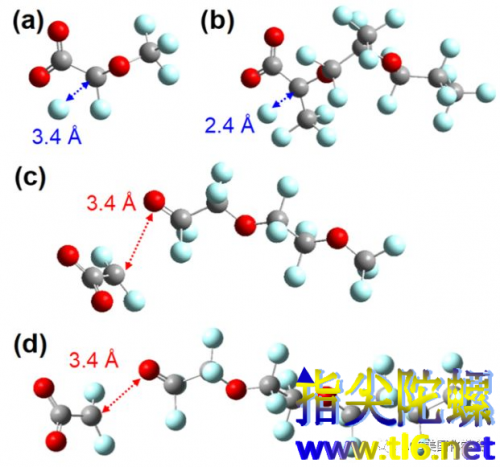
图5.外加一个电子进行结构优化后C−F与C−O的自动解离
以上理论很好地解释了各种PFECA降解速度和脱氟率的不同。
以B类的三个分子为例(图6),B2和B3中被醚氧分隔的氟碳链较长,α位的C−F键比B1弱(图3),因此H/F原子交换反应的速率显著加快,使得降解速率与同样带有这种α位弱C−F键的纯碳链羧酸几乎相同。
相比之下,B1中的孤立α位碳原子上的C−F键能显著高于B2和B3,导致其通过H/F原子交换的降解变慢。
但是,B1的脱氟率高达91%。
因此,高脱氟率最可能的原因是eaq−引起的C−O键断裂:无论PFECA分子中的C−F键能有多高,都会经由全氟醇的自发分解而脱氟。

图6.三个B类PFECA分子的降解(a)和脱氟(b)
至于B1仍然没有达到100%的脱氟率,则可以归结于α位碳原子上的H/F交换反应。
我们之前的研究(10.1021/acs.est.8b06648)已经发现,如果RF−CF2−C(O)O−被还原为RF−CH2−C(O)O−,也就是全氟的RF基团失去与羧基的直接连接,后续的降解反应将难以进行,由此导致脱氟不完全。
我们对B1的一个多氟类似物CF3−O−CH2−C(O)O−进行了降解测试,果然测得大幅降低的速率,但同时发现其降解的部分有接近100%的脱氟率,说明这是依靠反应速率较慢的C−O键断裂生成三氟甲醇,然后三氟甲醇快速完全地脱氟。
因此我们提出,对PFECA的深度脱氟降解有利的反应途径是C−O键断裂,而α位碳原子上的H/F交换则会迟滞后续的降解反应。
这一假说可进一步被其他几组PFECA的实验结果所支持。
例如具有侧链和最弱三级C−F键的A类分子,α位碳原子上的H/F交换最易产生,因此一定时间后的总体脱氟率(31−45%)比纯碳链羧酸(55%)还要低。
而C类和D类的比较则表明,C类的末端CF3−O−会通过三氟甲醇中间产物全部脱氟,而D类的末端C4F9−O−会通过相同的反应机理得到纯碳链羧酸C2F5−CF2−C(O)O−。
这样的结构因为容易发生α位碳原子上的H/F交换而不能完全脱氟。
因此,C类的总体脱氟率(75−82%)高于D类(58−65%)。
基于上述发现,我们提出对于PFECA的深度脱氟最有利的分子结构是醚氧原子将氟碳链分隔得尽可能短。
这样的结构含有显著增强的C−F键,从而抑制对深度脱氟不利的H/F交换反应。
同时,由于末端羧基的诱导而进行的C−O键断裂和全氟醇的自发分解可以切断所有成醚碳原子上的C−F键。
我们期待这些发现可以帮助进一步提高PFECA的脱氟降解处理效率,以及在不改变应用性能的前提下设计更容易被还原降解的氟化物结构。
需要额外强调的是,虽然现在已有呼吁全面禁止全氟化物的生产和使用,但这一目标在短期之内难以实现。
因此,深入研究全氟化合物的降解特性,从污染修复和化工生产的角度都对环境保护具有积极的意义。
本研究的相关结果已发表于EnvironmentalScience&Technology,并入选ACSEditors'Choice。
本项目得到了加州大学河滨分校(UCR)启动经费、美国自然科学基金(NSF)和战略环境研究与发展项目(SERDP)的支持。