科学家用碳原子把“积木”搭得出神入化
你可能听说过很多非常高端的类似于石墨,碳纤维的碳材料,也还有石墨烯、碳纳米管,富勒烯之类的碳纳米材料,要是再了解多一些,你可能还听过石墨炔、T-碳等的碳材料,一个“碳”原子真的很百变。

实际上碳元素在我们生活中无处不在,作为“碳基生物”,碳元素是所有组成人体的元素中第二多的元素,也是地球上生命体的基本骨架。

苯环结构
最近新鲜核桃成熟了,核桃这么坚硬又别致的小东西,在小编的手下被夹碎,恰核桃也是非常地快乐。核桃皮中就有大量的木质素,大约占50%以上的成分。而木质素恰恰就拿捏着核桃皮中最坚硬的部分。
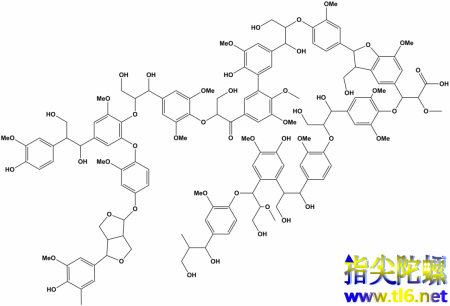
图|某一种植物中的木质素biooekonomie-bw.de
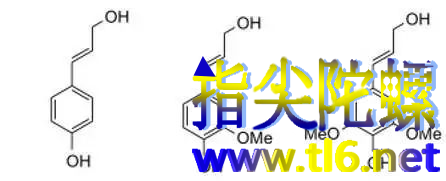
先别急着晕,木质素是一堆乱七八糟的五元环、六元环,但实际上也就是三种单体“手拉手”连接起来的一种有机物。你可以就当玩一个拼图游戏,把下面的三个单体,依次拼到上面的大分子木质素中,虽然不能完全对应,毕竟真正木质素中总会有一些其他的小枝杈(官能团)在里面。
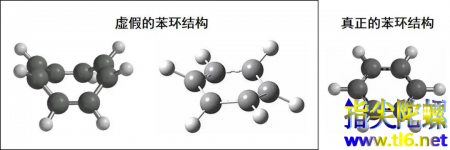
不过话说回来,为什么核桃这么硬呢?苯环在木质素中的存在赋予了它比较坚硬的特性。德国化学家凯库勒(Kekule)在1858年提出的碳原子之间以单双键交替的形式,首尾相连形成了六元环。虽然后来证明这种形式是错的(应该是π-π共轭),但是在书写时,这样的形式被保留了下来。
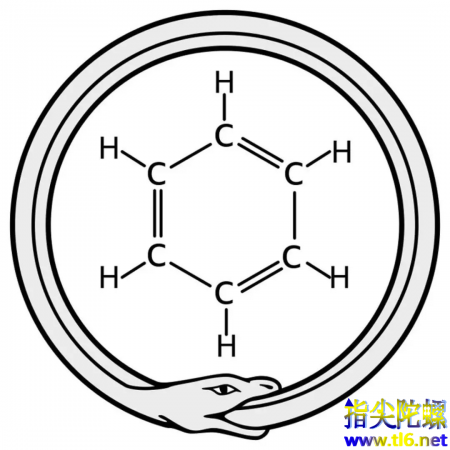
图| 凯库勒梦到的苯环分子式来源:baike.baidu.com
苯环中碳原子和碳原子之间连接的稳定性不同于链状分子之间的稳定性。这主要是在苯环中碳原子是以sp2杂化的方式连接在一起的,链状分子更多是sp3杂化,sp2杂化的形式会更稳定,而且连接起来离域的电子能够导电。
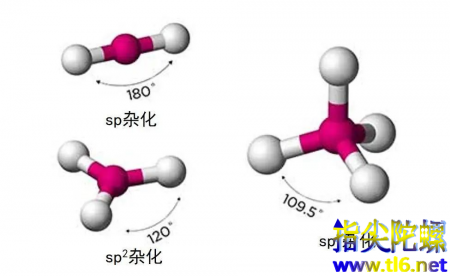
图| 碳原子的不同构型来源:Britannica.com
所以形成苯环之后就成了平面的结构,
这种结构的苯环上自由度更高的离域电子就会分布在苯环的两侧,在如图两个环的区域内。
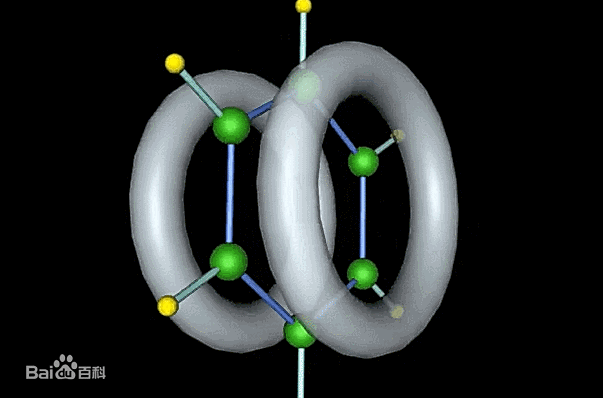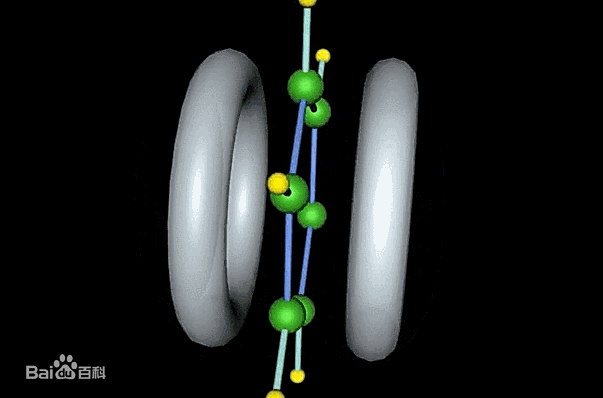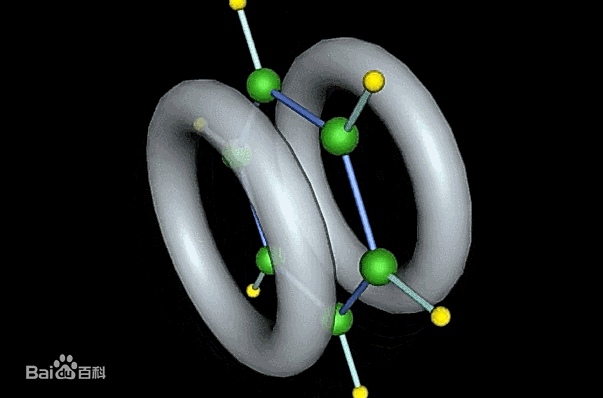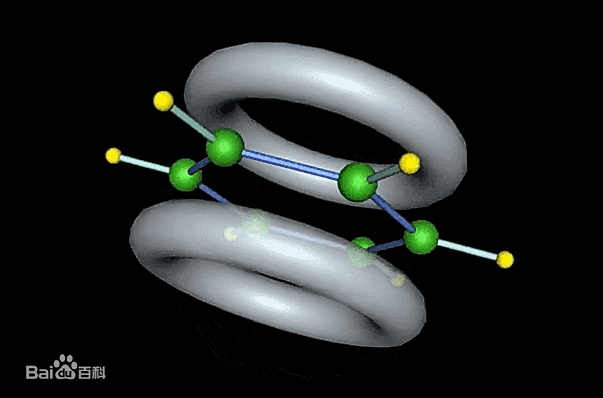
图| 苯环离域电子结构来源:baike.baidu.com
要是苯环上的六元环周围也是六元环,那就是我们常听说的石墨烯了。
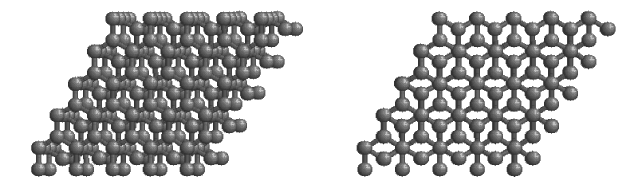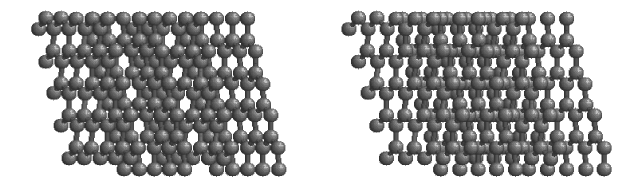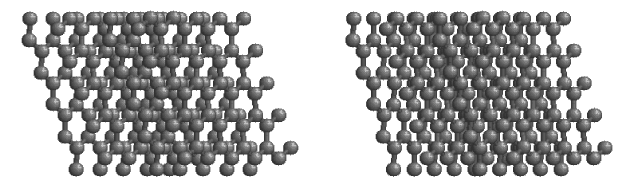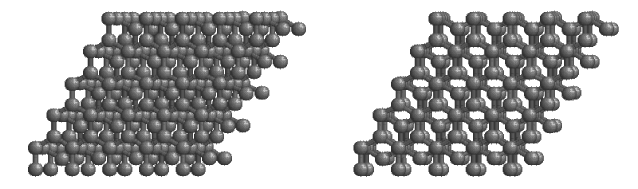
图| 四层石墨烯
石墨烯要是能卷成一个筒,那就是碳纳米管。
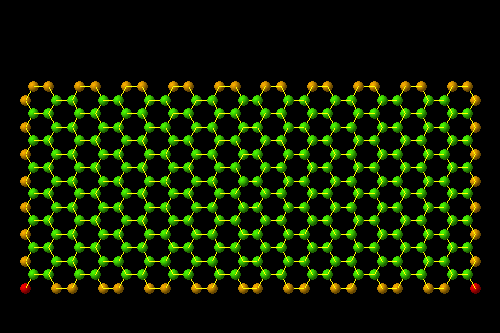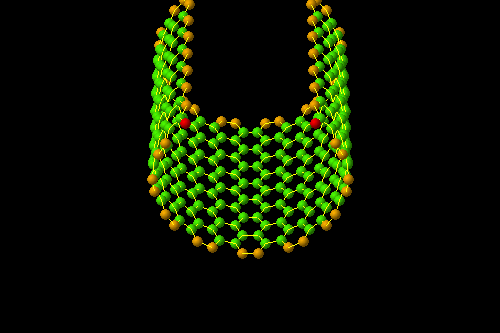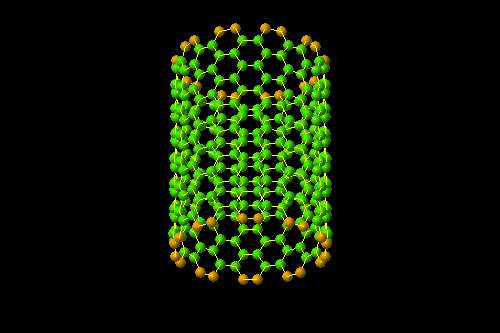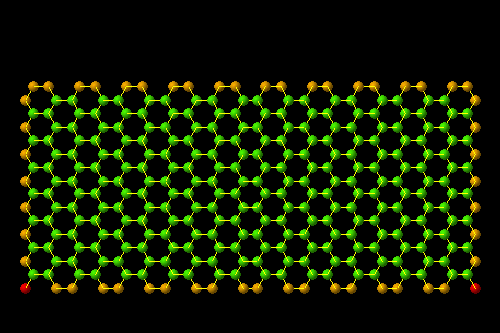
图| 碳纳米管来源:users.skynet.be


来用碳原子搭积木吧
以上都是小学三年级的知识,但是碳化学这门学科里的科学家,可是把碳原子玩的出神入化。如果把碳材料按照几何形状来分,可以分成零维、一维、二维,三维。
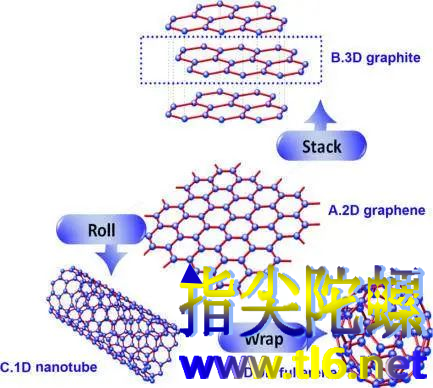
图| 将二维石墨烯揉一揉、卷一卷、叠一叠可以得到三个维度的碳材料来源:sciencedirect.com
如零维的富勒烯。1985年英国的克罗托(HaroldKroto)和美国柯尔(RobertCurl)及斯莫利(RichardSmalley)三位科学家制备出了由60个碳原子组成的C60,属于我们常听说的富勒烯。他们三人在1996年分享了诺贝尔化学奖。
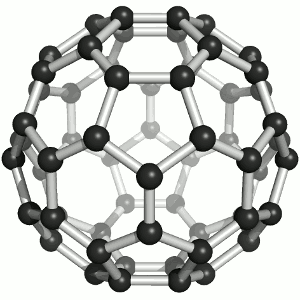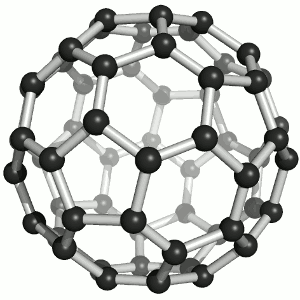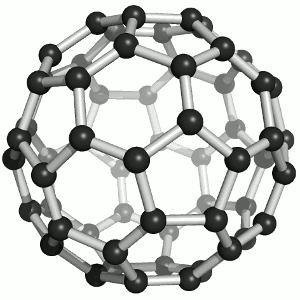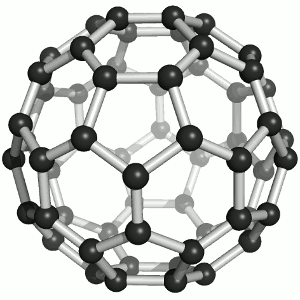
图|C60结构来源:c60purplepower.com
此外还有其他形式的富勒烯。
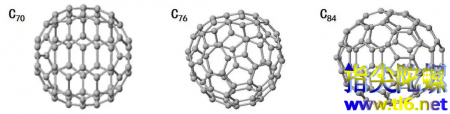
C60由20个六元环和12个五元环组成,组成了二十面体对称封闭的笼型结构。虽然说富勒烯是石墨烯团成的球形结构但是C60中由于五元环的存在,在五元环的部位倾向于吸电子,够对富勒烯进行多种加工,形成功能化的富勒烯,可以运用于催化、光学、储能等领域。
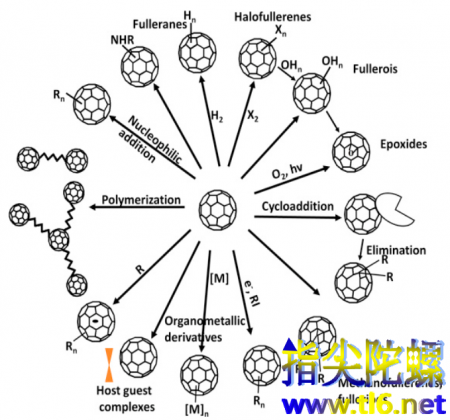
图| 不同功能化的C60 来源:sciencedirect.com
要是说零维材料,那纳米碳点也应该拥有姓名,这类材料实际上就是将大面积的石墨烯或者碳纳米管和金刚石等,分散成一种类球状的颗粒,这类材料具有非常独特的光学性能。
在一维层面,最有代表性的就是碳纳米管了,前几年小编听人们对碳纳米管获得诺贝尔奖的呼声也很高,主要就是因为碳纳米管有很好的机械性能、导电性、耐热性,在传感器、储氢、电化学等领域都有很广的用途。它是1991年由日本Iijima博士发现的。
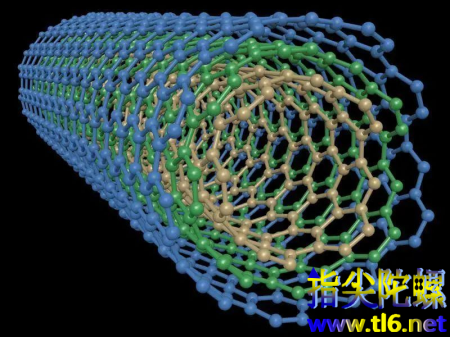
图| 多壁碳纳米管来源:网络
碳纳米管的确和石墨烯的结构挺像的,管壁上都是六元环。实际上碳纳米管就是石墨烯卷一卷,有时候还会多层碳纳米管套娃在一起。电子能够在管壁上移动的非常快,纳米管兼具金刚石的硬度和良好的柔,但是与石墨烯不同的是只能在管径方向上有很高的电子电导率性。

图| 石墨烯结构示意图来源:cas.cn
到了二维的层面,碳原子这块积木就更多变了,首先就是最具代表性的石墨烯。2004年英国科学家安德烈·盖姆(AndreGeim)和康斯坦丁·诺沃肖罗夫(KonstantinNovoselov)发现了石墨烯,没等几年,在2010年反手就拿了个诺贝尔物理学奖。
石墨烯结构中,电子可以在石墨烯上进行远距离的移动,具有良好的机械性能,导电性和导热性等。石墨烯在我们铅笔里面存在的形式就是石墨,通常情况下单层石墨烯是不太容易制得的,拿个胶带过来粘一粘铅笔芯,顶多获得是多层石墨烯,要是有谁说这样能获得大量单层石墨烯,你就一巴掌拍死他。
还有石墨炔,石墨炔的结构中相比之前介绍的材料,多了一类sp杂化的碳原子,也就是这类碳原子只有两只拉其他原子的手,呈直线形排列,这类碳原子链接起来就叫炔键。石墨炔则是由苯环和炔键连接在一起形成的,区别就在于,有的苯环之间是两个炔键(石墨二炔),有的是一个炔键(石墨一炔),当然有的还有更多的炔键。2010年首次由李玉良院士合成出来。
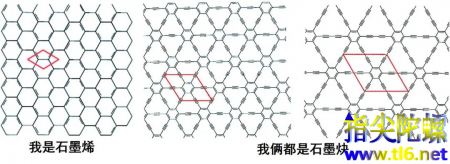
这种二维碳材料具有半导体的性质,也有很高的硬度和韧性,能够在太阳能电池,电化学传感器储能等方面有应用。
除了以上的这些二维碳材料,还可以从石墨烯中衍生出来更多的二维碳材料。他们共同的特点就是都含有环类结构,碳原子是以有三只手的sp2和有两只手的sp杂化方式排列的。
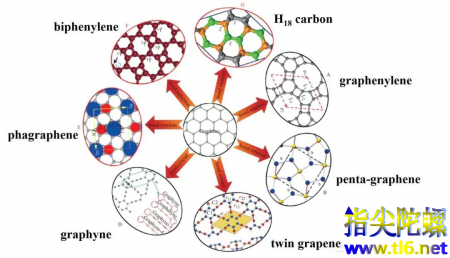
图| 其他的二维碳材料(为了避免科学性问题,小编就不翻译了,其实是懒)来源:springer.com
最后再说到三维上,那碳原子就能伸出四只手了(sp3杂化),那最有代表性的就是金刚石和石墨了。金刚石(钻石)具有碳材料中最高的硬度,里面的碳原子手拉手就可以形成规则的晶体结构。
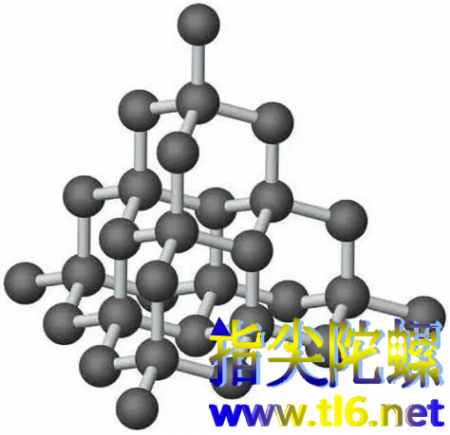
图| 金刚石结构
而石墨也是很常见的材料,是铅笔芯的主要成分,它是由石墨烯一层一层按照特定位置,堆叠起来的三维结构,层与层之间是范德华力。所以在层与层之间可以很轻松的相对滑动,通常还用做润滑剂,小编家里面要是钥匙和锁之间配合的不太顺畅的时候,就会灌点铅笔芯粉末,保证丝滑。
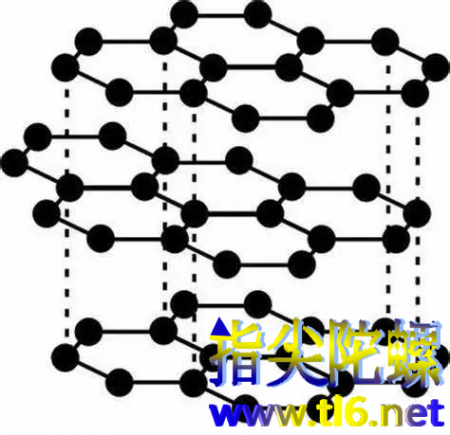
图| 石墨结构
在碳原子搭建的三维结构里面还有好多种,下面只是列出的其中的一小部分,其中圈出来的灰色区域的部分属于有金属性的碳材料,也就是有良好的导电性。红色区域的部分属于硬碳材料,具有比较高的硬度。可以很明显的看出有金属性的材料更多是有两只手的sp杂化和三只手的sp2杂化,而硬碳材料更多是有四只手的sp3碳原子。
其中T-碳的发现非常成功地经历了,从2011年的理论预测出这种新型三维碳结构,再到2017年在实验室中成功合成的过程。
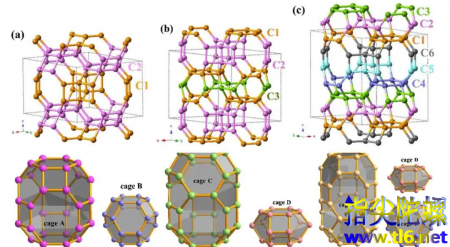
图| 2020年一项工作中理论预测的具有笼装结构的三种三维碳骨架架构,下面是六种单体来源:iopscience.iop.org
不仅如此,科学工作者还在不断地预测和合成新的同分异构体材料,为碳家族不断添入新的成员,未来诺贝尔奖会不会继续有机会颁给碳材料的工作呢,小编想是肯定的~
参考文献:
[1] Fullerenes(AnOverview)-ch.ic.ac.uk
[2] 碳家族添新丁:我科学家预言的T-碳问世-观察者网
[3]碳纳米点-baike.baidu.com
[4] 郑志锋, etal.核桃壳化学组分的研究[J].西南林业大学学报(自然科学),2006,26(2):33-36.
[5] ZhangRS,JiangJW.Theartofdesigningcarbonallotropes[J].Frontiersofphysics,2019,14(1):13401.1-13401.17.
[6] Zhang W, etal. Sixnovelcarbonandsiliconallotropeswiththeirpotentialapplicationinphotovoltaicfield[J]. Phys:Condens.Matter, 2020,32, 355701(1-10).[7] 吴凯.功能纳米碳点"照亮"应用征途[J].物理化学学报,2019(6).
[8] Xian-Lei,Sheng,Qing-Bo,等.T-Carbon:ANovelCarbonAllotrope[J].PhysicalReviewLetters,2011.
[9] HaihongB,LeiW,ChaoL,etal.StructuralCharacterizationandIdentificationofGraphdiyneandGraphdiyne-BasedMaterials[J].ACSAppliedMaterials&Interfaces,2018,11:acsami.8b05051-.